서 언
재료 및 방법
시험 재료
과실 특성
총 안토시아닌 함량
총 폴리놀 함량
안토시아닌 조성 분석
항산화활성(DPPH radical 소거활성) 분석
통계분석
결과 및 고찰
과실 특성
안토시아닌, 페놀 함량 및 DPPH 라디컬 소거능
적 요
서 언
소과류와 베리류는 페놀화합물인 안토시아닌, 플라보노이드 등 생리활성물질을 다량 함유하고 있어(Kylli et al., 2011; Määttä-Rihinen et al., 2005; Shin et al., 2014) 강한 항산화 작용을 하며 항암, 항당뇨, 항균, 항염 등에도 효과가 있는 것으로 알려져 있다(Battino et al., 2009; Gruia et al., 2008; Jeong et al., 2007; Jurikova et al., 2012; Tabart et al., 2012). 최근의 연구에 의하면 과실이나 채소의 섭취는 암이나 심장마비와 같은 질병의 위험을 감소시킨다고 보고하고 있다(Ferreyra et al., 2007). 항산화제의 능력은 주로 자유라디칼에 대한 높은 반응성으로 자유라디칼의 활성을 중성화시키기 때문이다. 이러한 항산화제는 크게 superoxide dismutase나 glutathione peroxide와 같은 항산화 효소, 페놀성 화합물(catechine, flavonols, anthocyanins 등) 및 비타민류(C, E, A) 등으로 나눌 수 있다(Fang et al., 2002). 최근 과실의 소비가 과거 6대 과수 중심에서 벗어나 다양해지면서 간편하게 먹을 수 있으면서 기능성이 높은 블루베리를 포함한 각종 베리류와 소과류 등으로 확대되면서 국내 재배도 급격히 증가하고 있다.
블루베리는 기능성과 이용성, 가공성이 뛰어나(Kim et al., 2017b) 국내 재배도 꾸준히 증가하여 2018년 기준 3,576.5 ㏊ (Ministry of Agriculture, Food and Rural Affairs, 2018)를 차지하는 베리류로 국내 소과류 및 베리류 중에서 가장 많이 재배하는 과종이다. 흔히 아로니아라 불리우는 블랙 쵸크베리(Aronia melanocarpa)의 원산지는 캐나다와 북아메리카 동부로 습지 혹은 절벽 등에서 자생하고, 현재 폴란드, 러시아, 오스트리아 그리고 체코 등 다양한 국가에서 재배되고 있다(Kask, 1987). 쵸크베리는 환경적응성이 뛰어나(Bussières et al., 2008) 재배가 용이하고 높은 안토시아닌 함량을 함유하고 있는 것으로 알려지면서 최근 국내 재배면적이 2018년 기준 약 4,190.8 ㏊로 급속히 증가하고 있다(Ministry of Agriculture, Food and Rural Affairs, 2018). 소과류 중에서 사스카툰베리는 추위에 강하며 재배가 쉬워 국내에 도입된 과실이며 커런트는 국내 재배면적이 2018년 기준 약 428 ㏊를 차지하는 베리류이다(Ministry of Agriculture, Food and Rural Affairs, 2018).
이에 국내에서 유망 소과류 및 베리류로 농가에 보급되고 있는 품종들을 대상으로 각 과실들 간의 안토시아닌 및 폴리페놀 함량 및 구성성분의 차이를 알아보고 기능성 및 식품 개발의 기초 자료로 활용하고자 실험을 수행하였다.
재료 및 방법
시험 재료
농촌진흥청 원예특작과학원 완주 과수 포장에서 재배되고 있는 블루베리 ‘Duke’, ‘Bluecrop’, ‘Elliott’ 3 품종, 블랙 쵸크베리(black chokeberry, aronia), ‘Nero’, ‘Viking’, Mackenzie 3 품종, 사스카툰베리(saskatoonberry) ‘Northline’, ‘Smoky’ 2 품종, 블랙커런트(black currant) ‘Titania’ 1 품종 등 총 4 과종 9 품종을 대상으로 적숙기에 수확한 과실을 대상으로 하였다. 과실 특성은 수확 후 바로 실시하였으며, 안토시아닌 및 폴리페놀 분석은 –25℃에서 분석 전까지 보관 후 사용하였다.
과실 특성
과실은 과실의 길이, 과실의 너비, 중량, 가용성고형물 함량, 산도, 경도, 안토시아닌 함량 등을 조사하였다. 각 품종별 무작위로 추출한 과실 30개를 대상으로 과실의 길이, 너비, 과립중을 조사하였다. 가용성고형물(total soluble solids, TSS) 함량은 무작위로 10개의 과립을 선택하여 거즈 2겹을 이용하여 착즙한 20℃로 자동 보정되는 digital refractometer (RA-520N, Kyoto Electronic, Japan)를 사용하여 측정하였다. 적정산도(titratable acidity, TA)는 동일한 과즙을 자동산도분석계(Titroline easy, Schott, Germany)를 이용하여 측정한 후 블루베리 주요 산인 citric acid 함량으로 환산하여 표기하였다. 가용성고형물 함량과 산 함량은 총 4반복으로 측정하였다. 과실 경도는 1 ㎜ 직경의 probe를 장착한 물성측정기(LF Plus, Lloyd Instrument Ltd., West Sussex, UK)를 이용하여 측정하였다.
총 안토시아닌 함량
총 안토시아닌 함량은 두개의 반응 시약 pH 1.0 potassium chloride buffer (0.025M)와 pH 4.5 sodium acetate buffer (0.4M)의 pH 차에 의한 검정법으로 Benvenuti et al. (2004)의 분석 방법을 인용하여 수행하였다. 두 개의 반응 시약에 추출물 20 μL에 각각 넣고 실온에서 10분 반응시킨 후, 기능 흡광분석기(Multiskan Go microplate, ThermoScientific, North Carolina, USA)를 사용하여 510 ㎚와 700 ㎚에서 흡광도를 측정하였다. 측정값 A는 A = (A510-A700)pH1.0-(A510-A700)pH4.5의 계산식에 대입하여 구하였으며, 표준물질 cyanidin-3-glucoside (Sigma Co., USA)를 사용하여 얻은 검량선으로 총 안토시아닌 함량을 계산하였다.
총 폴리놀 함량
폴리페놀 함량 분석 Folin-Ciocalteu 분석법을 인용하여 수행하였다(Mazza et al., 1999). 추출액 80 μL에 Folin-Ciocalteu reagent 시약 20 μL을 첨가하여 실온에서 5분간 반응시킨 후, 2% sodium carbonate 용액 100 μL를 추가로 첨가하여 10분간 반응시킨 후 다기능 흡광분석기(Multiskan Go microplate, ThermoScientific, North Carolina, USA)를 사용하여 750 ㎚에서 흡광도를 측정하였다. 표준물질 Gallic acid (Sigma Co., USA)를 사용하여 검량선을 작성하여 총 폴리페놀 함량을 계산하였다.
안토시아닌 조성 분석
안토시아닌 분석은 동결된 블루베리 시료를 액체질소를 이용하여 막자사말로 분쇄하여 균질화한 후 시료로 사용하였다. 시료 0.5 g을 50 mL의 Falcon tube에 넣은 후 10% formic acid/MeOH 용액 10 mL를 넣어서 암소에서 24시간 동안 추출하였다. 추출물은 원심분리(4,000 rpm, 10℃, 10분)를 하여 상층액을 취한 후 0.2 ㎛ nylon syringe filter로 여과하였다. 분양받은 표준물질 1,000 ㎎ L-1의 stock solution을 증류수로 희석하여 혼합 표준용액을 만든 후, 0.1, 0.5, 1.0, 5.0, 10.0, 20.0 ㎎ L-1의 working standard solution을 만들었다. 각각 5 μL씩 HPLC에 주입하여 나타난 크로마토그램상의 피크면적을 기준으로 검량선을 작성하였다.
항산화활성(DPPH radical 소거활성) 분석
항산화 활성은 DPPH (2,2-diphenyl-1-picrylhydrazyl)를 이용한 자유라디칼 소거능법에 의해 측정하였다(Hosu et al., 2014; Iacopini et al., 2008). 시료 추출물은 5단계로 희석하여 사용하였다. 각각의 시료 추출물에 10 μL에 DPPH 반응시약 290 μL를 첨가하여 실온에서 20분 반응시켰다. 반응 후 다기능 흡광분석기(Multiskan Go microplate, ThermoScientific, North Carolina, USA)를 사용하여 520 ㎚에서 흡광도를 측정하였다. 대조군은 Ascorbic acid를 사용하였으며, 시료의 DPPH radical 소거활성(RC50)은 각 시료의 추출물을 5단계로 희석하여 각 희석농도별 DPPH radical 소거활성을 구한 다음 이를 선형회귀법을 이용하여 대조군(ascorbic acid)의 흡광도를 50% 감소시키는데 필요한 각 시료의 가용성 고형분의 농도(㎎・mL-1)로 나타냈다.
통계분석
모든 실험구는 완전임의배치법 3반복으로 하였고, 실험 결과의 통계 처리는 SAS 프로그램(SAS Institute, Cary, NC, USA)을 사용하여 분산분석(ANOVA)을 하였고, 처리간 유의차 검증은 Duncan’s multiple range test를 사용하여 0.05% 수준에서 검증하였다.
결과 및 고찰
과실 특성
4과종 9개 품종의 만개기는 과종이나 품종에 상관없이 4월 중순으로 조사되었다(Table 1). 수확 개시기는 블루베리, 사스카툰베리는 6월 상순, 블랙 커런트는 6월 중순, 블랙 쵸크베리는 가장 늦은 7월 중순부터 수확이 시작되었다(Table 1, 또는 Fig. 1). 충북 지역의 블랙 쵸크베리 수확일은 8월 상순인데 비해 전주 지역에서는 한달 정도 수확이 이른 것으로 조사되었다(Won et al., 2018).
Table 1. Growth period of small fruit and berries in orchard of Nation Institute of Horticultural & Herbal Science
과립중은 전반적으로 블루베리가 가장 무거워 평균 2 g 이상을 나타냈으며, 그 외 소과류는 평균 1 g 미만의 과립중이었다(Table 2). L/D율로 보아 과실 형태는 블랙 커런트 > 쵸크베리 > 사스카툰베리 > 블루베리 순으로 원형에서 평원형에 가깝게 나타났다(Table 2, 또는 Fig. 1). 블랙 쵸크베리는 다른 소과류인 사스카툰베리와는 달리 과육까지 붉은 색을 띄고 있었으며, 과실 경도가 다른 과종에 비해 2~3배 가까이 높은 것으로 조사되었으며 완숙 후에도 경도가 오랫동안 유지되었다. 블랙 커런트의 과실 경도가 가장 낮은 것으로 조사되었으며 사스카툰베리는 수확 후 경도가 급속히 저하되었다. 과실 당도는 사스카툰베리의 경우 16.7~20.8o brix로 매우 높았으며, 블루베리와 블랙 쵸크베리는 10~13o brix로 비슷한 양상이나 블랙 쵸크베리의 떫은 맛 때문에 당도가 느껴지지 않았다. 블랙 커런트의 경우 당도가 14.8o brix로 높은 편이나 산도가 매우 높아 마찬가지로 당도가 느껴지지 않았다. 산도는 사스카툰베리가 0.4~0.6%로 가장 낮았으며, 블루베리(0.6~0.9%), 블랙쵸크베리(1.5~1.6%), 블랙커런트(4.0%) 순으로 높았다.
Table 2. Fruit characteristics of small fruit and berries in orchard of Nation Institute of Horticultural & Herbal Science
안토시아닌, 페놀 함량 및 DPPH 라디컬 소거능
4과종 9개 품종의 총 안토시아닌 및 폴리페놀 함량을 분석한 결과, 같은 과종에서도 품종에 따라 안토시아닌과 폴리페놀 함량의 차이가 나타났으며, 총 안토시아닌은 블랙 쵸크베리가 가장 많았으며(927.9~1,149.1 ㎎・100 g-1, F.W.), 총 폴리페놀 함량도 블랙 쵸크베리(502.2~530.5 ㎎・100 g-1, F.W.)에서 가장 많았다(Table 3). 블랙 쵸크베리의 경우 다른 과실과는 달리 과육까지 붉은 색으로 착색되어 있기 때문에 단위당 안토시아닌 함량이 높았으며, 페놀 화합물 함량도 높은 것으로 판단되었다. 일반적으로 항산화 활성이 증가함에 따라 총페놀 함량도 증가하는데 본 실험 결과에서도 과종별 품종별 안토시아닌 함량과 페놀 함량과는 비슷한 양상을 보였다(Table 3). 안토시아닌 함량은 사스카툰베리 ‘Smoky’가 가장 높게 나온 블랙 쵸크베리 ‘Mackenzie’에 비해 약 23% 수준의 안토시아닌 함량을 가진 것으로 조사되었으며 블루베리의 경우 품종에 따라 블랙 쵸크베리의 29~59% 수준의 안토시아닌 함량을 가진 것으로 조사되었다. 페놀성 화합물의 주요한 역할은 자유 라디컬을 소거하는 것이라는 많은 관련 연구 보고가 있으며(Madsen et al., 1996; Moller et al., 1999), 페놀성 화합물인 플라보노이드와 안토시아닌 등의 총량인 총페놀 함량은 DPPH 라디컬 소거능으로 나타내는 항산화 활성에서 중요한 인자로 작용한다. DPPH 라디컬 소거능을 조사한 결과 블랙 쵸크베리에서 가장 높게 나타났으며, 블랙 커런트 > 사스카툰베리 = 블루베리 순으로 안토시아닌, 페놀 함량 경향과 비슷하게 조사되었다.
Table 3. Total anthocyanin and polyphenols contents and DPPH radical scavenging of small fruit and berries in orchard of Nation Institute of Horticultural & Herbal Science
yMilligrams of total polyphenol contents per gram of fresh weight based on naringin as standard.
xConcentration of the material which is required to scavenge 50% of 0.15 mM DPPH radicals at 30 min. after starting the reaction.
wValues are mean separation within columns by Duncan's multiple range test, p<0.05.
총 안토시아닌, 폴리페놀과 DPPH 항산화 활성간에는 유의한 상관관계가 있었다(Table 4). 특히 DPPH과 총 안토시아닌간에는 고도로 유의한 상관관계(r=0.7669**)가 있었으며, 총 폴리페놀과는 고도로 고도로 유의한 상관관계(r=0.8956***)가 있었다. 이는 일반적으로 안토시아닌과 항산화활성과 강한 상관관계가 있다는 연구(Awika et al., 2004)와 폴리페놀은 항산화 활성과 깊은 관련이 있다는 연구(Yen and Chen, 1995)와 일치했으며, 이것은 폴리페놀이 자유 라디칼에게 수소원자를 공급함으로써 발생하는 결과이다(Madsen et al., 2000; Park et al., 2007).
Table 4. Correlation coefficients of DPPH antioxidant activity with total anthocyanin and polyphenol content of small fruits and berries
| Factor | DPPH | Total anthocyanin | Total Phenols |
| DPPH | - | 0.7669** | 0.8956*** |
| Total anthocyanin | 0.7669**z | - | 0.6984** |
| Total polyphenol | 0.8956*** | 0.6984** | - |
주요 폴리페놀 구성 성분을 조사한 결과 모든 과종에서 quercetin, catechin, epicatechin 함량이 높게 나타났다(Table 5). Quercetin과 catechin류는 혈중의 콜레스테롤 저하(Suzuki et al., 1998), 혈압 저하(Edwards et al., 2007; Huang et al., 1998), 혈당 강화(Chakravarthy et al., 1982) 등의 약리작용이 있으며, 항산화작용(Boots et al., 2011; Lotito and Fraga, 1998), 항균 작용(Ikigai et al., 1993), 항암 작용(Fujiki et al., 1998; Wang et al., 2012) 등에 효과가 있는 것으로 보고되고 있다(Oh and Koh, 2005). 폴리페놀 물질은 모든 과종에서 다양하게 골고루 분포하고 있었으며, quercetin, catechin은 블루베리와 사스카툰베리에서 epicatechin은 사스카툰베리에서 가장 많이 함유되어 있었으며, 블랙 쵸크베리, 블랙 커런트에서는 비슷한 함량을 보였다.
Table 5. Polyphenol components of small fruit and berries in orchard of Nation Institute of Horticultural & Herbal Science
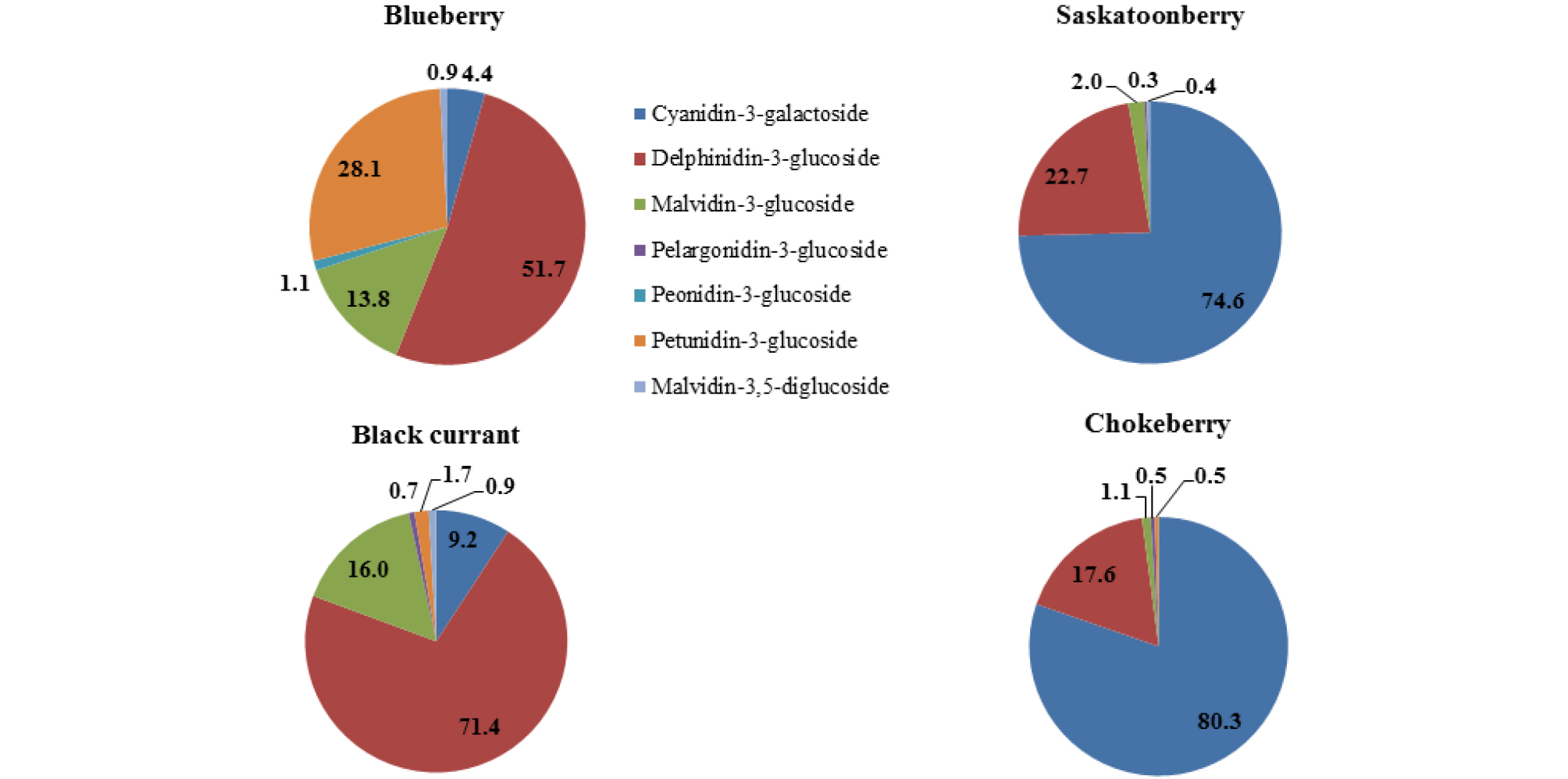
주요 안토시아닌 조성은 과종에 따라 차이를 보였는데 블루베리와 블랙 커런트의 주요 안토시아닌은 delphinidin-3- glucoside로 전체 안토시아닌 중 52~71%를 차지였으며, 사스카툰베리와 블랙 쵸크베리의 주요 안토시아닌은 cyanidin-3- galactoside로 75~80%를 함유하고 있었다(Fig. 2). 블랙 쵸크베리의 주종 안토시아닌은 다른 연구결과에서도 cyanidin-3- galactoside로 보고된 바 있다(Kim et al., 2017a). 안토시아닌 조성도 블루베리와 블랙커런트는 6종, 사스카툰베리 5종, 블랙 쵸크베리는 cyanidin-3-galactoside와 cyanidin-3-arabinoside, cyanidin-3-xyloside, cyanidin-3-glucoside 등 4가지 종류의 안토시아닌으로 구성되어 있다(Slimestad et al., 2005)는 보고와는 달리 cyanidin-3-galactoside, delphinidin-3-glucoside, malvidin-3-glucoside, pelagonidin-3-glucoside, petunidin- 3glucoside 5종으로 구성되어 있었다.
최근 국내에 과실의 특성이나 생식이 가능한 지 여부와 관련 없이 과종이 도입되는 등 도입에 철저한 검증이 이루어지지 않고 있는 실정이다. 실험에 사용한 주요 국내 재배 베리류인 블루베리, 블랙 쵸크베리, 사스카툰베리, 블랙 커런트 중에서 생식이 가능한 것은 블루베리와 사스카툰베리이며 블랙 커런트, 블랙 쵸크베리의 경우 재배 관리는 쉬운 편이나 과실 생과로 이용하기에는 과실 특유의 향과 떫은맛이 강하여 가공 제품에 기능성 증진 첨가물로 이용하는 것이 적합하다고 판단되었다. 국내에 소개되고 있는 소과류나 베리류는 기능성 과수로서 각광을 받고 있는 과종들이 대부분이다. 새로운 과종이 도입될 때마다 안토시아닌 및 폴리페놀 함량과 항산화활성의 데이터가 제시되고 있지만 다른 실험에 의한 결과를 같이 비교하여 데이터의 신뢰도가 높지 않다. 따라서 본 연구는 국내 베리류의 과종별 품종별 과실 특성과 안토시아닌, 폴리페놀, 항산화활성을 같은 방법으로 실험 분석 비교하여 객관적인 비교를 한 것으로 의미가 있다고 판단된다.
적 요
국내에서 유망 소과류 및 베리류로 농가에 보급되고 있는 과종 및 품종들을 대상으로 각 과실들 간의 안토시아닌, 폴리페놀 함량, 각 구성성분 및 항산화활성을 분석하였다. 총 안토시아닌 및 폴리페놀 함량을 분석한 결과, 같은 과종에서도 품종에 따라 안토시아닌과 폴리페놀 함량의 차이가 나타났으며, 총 안토시아닌은 블랙 쵸크베리가 가장 많았으며(927.9~1,149.1 ㎎・100 g-1, F.W.), 총 폴리페놀 함량도 블랙 쵸크베리(502.2~530.5 ㎎・100 g-1, F.W.)에서 가장 많았다. DPPH 항산화활성에서도 블랙 쵸크베리가 가장 높은 것으로 나타나 안토시아닌, 페놀 함량과 항산화활성과 고도의 상관관계를 나타냈다. 주요 폴리페놀 구성 성분을 조사한 결과 모든 과종에서 quercetin, catechin, epicatechin 함량이 높게 나타났다. 블루베리와 블랙 커런트의 주요 안토시아닌은 delphinidin-3-glucoside로 사스카툰베리와 블랙 쵸크베리의 주요 안토시아닌은 cyanidin-3- galactoside였다.